近日,河南师范大学新污染物生态效应与风险防控技术团队邹威和张杏丽老师在环境领域著名期刊《Environmental Science & Technology》上发表了题为“Suboptimal Thermal Storage Facilitates Aging of Bottle-Sourced Polyethylene Terephthalate Microplastics Fueling Hepatic Steatosis through Gut-Liver Axis Disruption”的研究论文。该研究首次揭示了瓶装水在运输与仓储过程中经历的不当高温储存(如夏季车厢内温度高达60℃),显著促进瓶源聚对苯二甲酸乙二醇酯(PET)微塑料(MPs)的热老化进程,致其明显碎片化、表面粗糙度与生物粘附力大幅提升。虽然微米级的PET极少直接进入肝脏,但老化后的颗粒在肠道内滞留量明显增加,其通过破坏肠道屏障、诱发菌群失调,激活LPS/TLR4/NF-κB通路引发全身性炎症,并经由肠-肝轴诱导肝脏炎症、胰岛素抵抗及脂肪从头合成,最终导致肝脏脂肪变性;膳食补充鼠李糖乳杆菌GG或丁酸钠,可通过恢复肠道菌群稳态、强化屏障功能,有效阻断肠-肝轴紊乱,显著减轻肝脏脂质累积与炎症损伤。研究结果系统阐明了热老化PET微塑料通过肠-肝轴诱发肝脏脂肪变性的毒性效应及作用机制,提出了靶向肠道微生态的肝脏代谢疾病缓解策略,呼吁关注不当储存条件下瓶源微塑料的长期暴露风险。
图文摘要
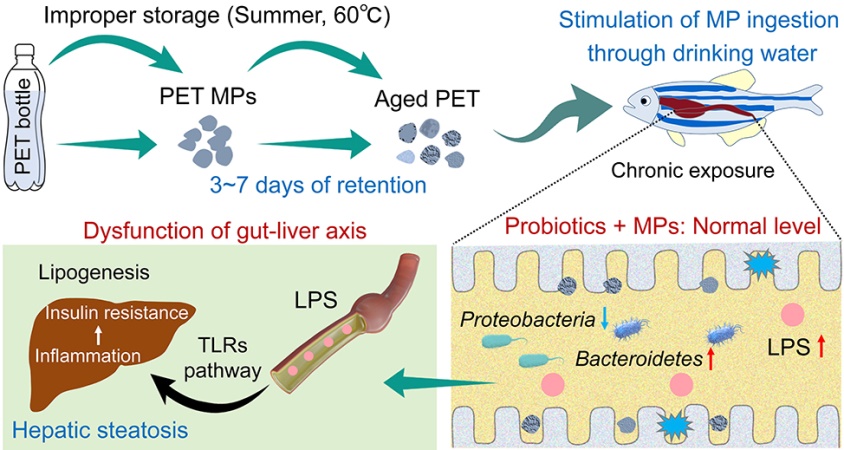
引言
PET是瓶装水与饮料包装的主要材料,其在使用过程中会向水体释放大量PET微塑料。调查显示,全球约90%的瓶装水中均检出高丰度的PET微粒,且PET已成为人体血液、动脉、心脏及粪便等样本中检出频率最高的微塑料类型,然而,其对公众健康的潜在威胁还不可知。瓶装水在长途运输或仓储过程中常不可避免地暴露于非理想高温环境,这种不当热储存将如何改变微塑料的理化性质与生物毒性,目前尚不明确。本研究模拟了瓶源PET微塑料在60°C(夏季不良高温储存环境)与16–25°C(理想储存环境)水体中分别滞留3天或7天的老化场景,系统探究了热老化进程中PET微塑料的理化特征变化及其诱发肝脏毒性的风险与机制。
图文导读
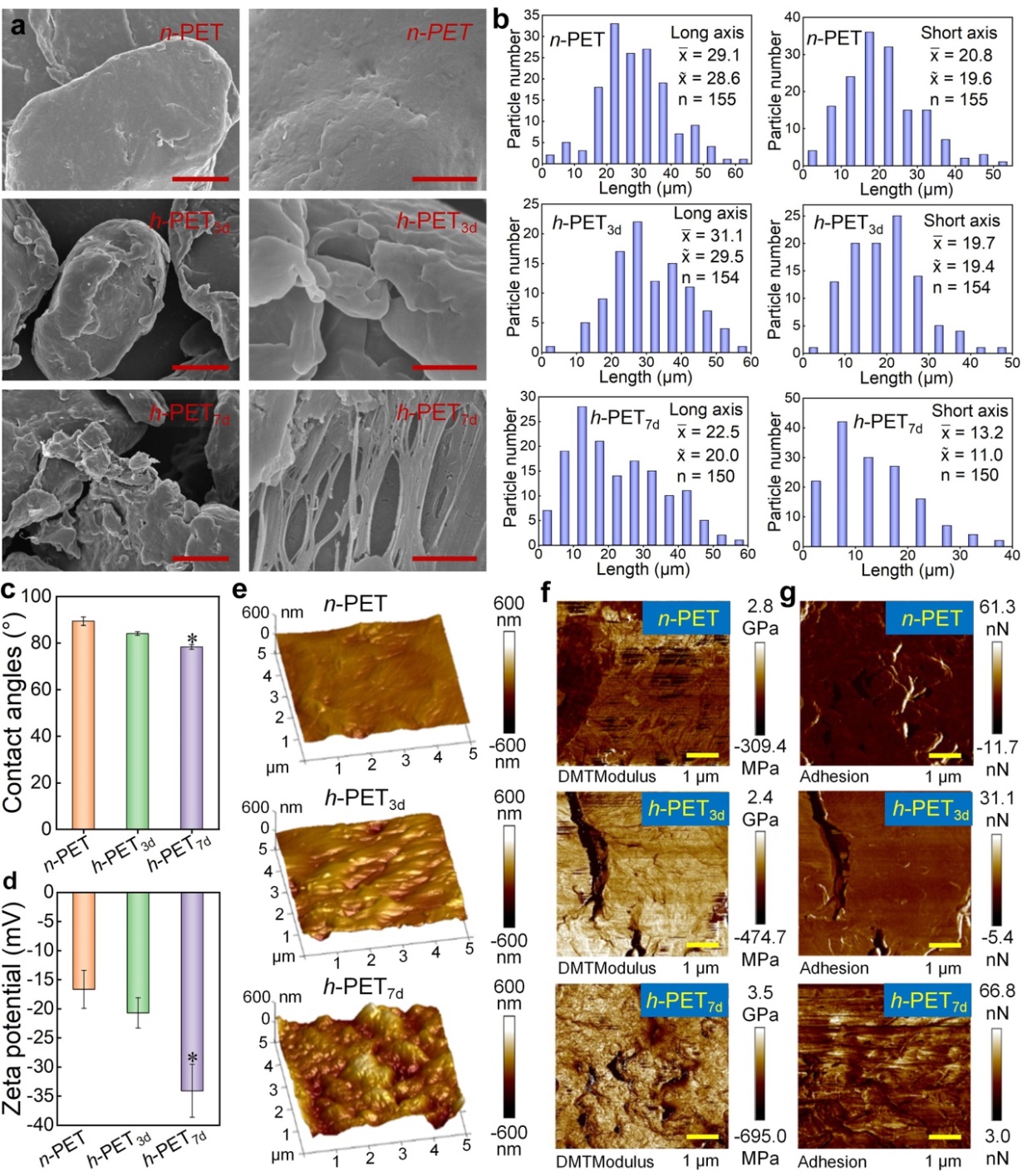
Fig. 1. Physicochemical characteristics of n-PET and h-PET.
通过扫描电镜、原子力显微镜、表面化学性质及亲疏水性表征发现,相较于理想储存环境中的PET微塑料(n PET),高温储存环境促使PET微塑料发生明显的老化降解,热老化后的PET颗粒(h PET7d)表面由相对光滑变为粗糙多孔,呈现明显的纤维状孔隙与尖锐边缘凸起,粒径显著降低,比表面积增加35.7%,表面粘附力提升至原来的2.03倍。接触角和表面电位明显降低,表明h PET7d的亲水性与水体稳定性增强。傅里叶变换红外光谱分析显示,h PET7d的羰基指数与表面C=O、O−C=O及C−O−C基团红外吸收峰的强度相对于n-PET出现了轻微的降低,表明高温水环境中PET主要通过酯键水解与脱羧作用发生了有限程度的化学降解。相对于温和的化学官能团变化,物理性质的显著变化——尤其是表面粗糙度与粘附力的大幅提升——是驱动后续肠道滞留加剧与生物毒性增强的关键物化基础,强调了高温储存环境驱动的物理性质变化在瓶PET微塑料健康风险中起主导地位。
h-PET通过引发炎症而非肝脏靶向富集诱导肝脂肪变性
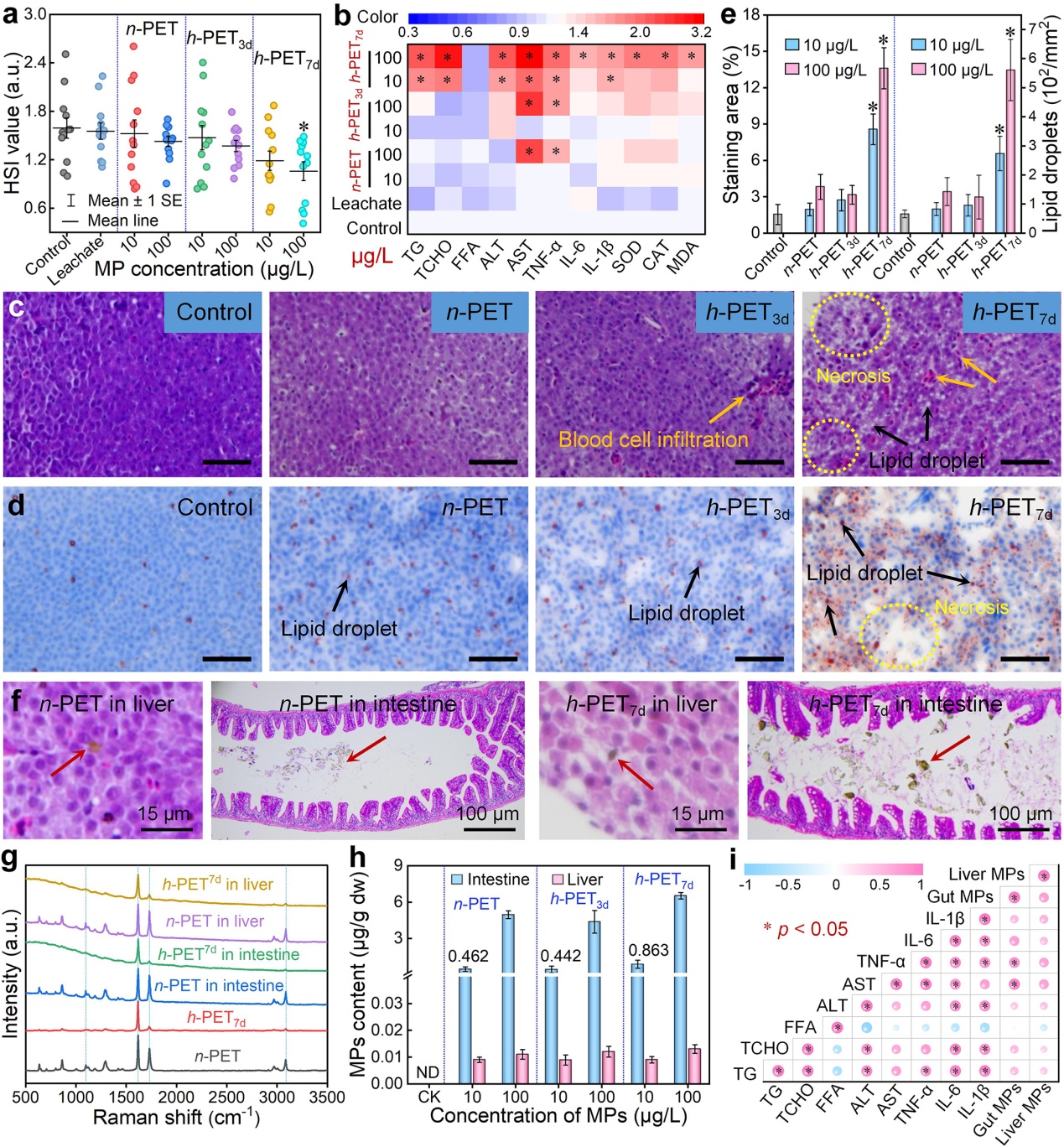
Fig.2. Health assessment of fish liver following exposure to n-PET and h-PET for 80 days.
长期暴露实验表明,h-PET7d在100 μg/L环境相关浓度下即可导致斑马鱼肝体指数下降,诱导明显的肝脏炎症、脂质沉积和组织坏死,而常温储存或短期老化的微塑料未表现出显著毒性。Py GC/MS定量分析进一步显示,PET微塑料主要蓄积于肠道组织,极少迁移至肝脏;其中h PET7d在肠道内的滞留量高达6.524 μg/g,显著高于n PET处理组。相关性分析表明,肝脏脂肪变性与炎症发生与肝脏内微塑料负载量无显著关联,而与肠道内PET蓄积量呈强正相关,提示热老化PET微塑料可能通过肠道间接途径(肠-肝脏轴紊乱)驱动肝脏病变。
h-PET诱导肠道菌群失调及屏障损伤、诱发LPS介导的全身性炎症
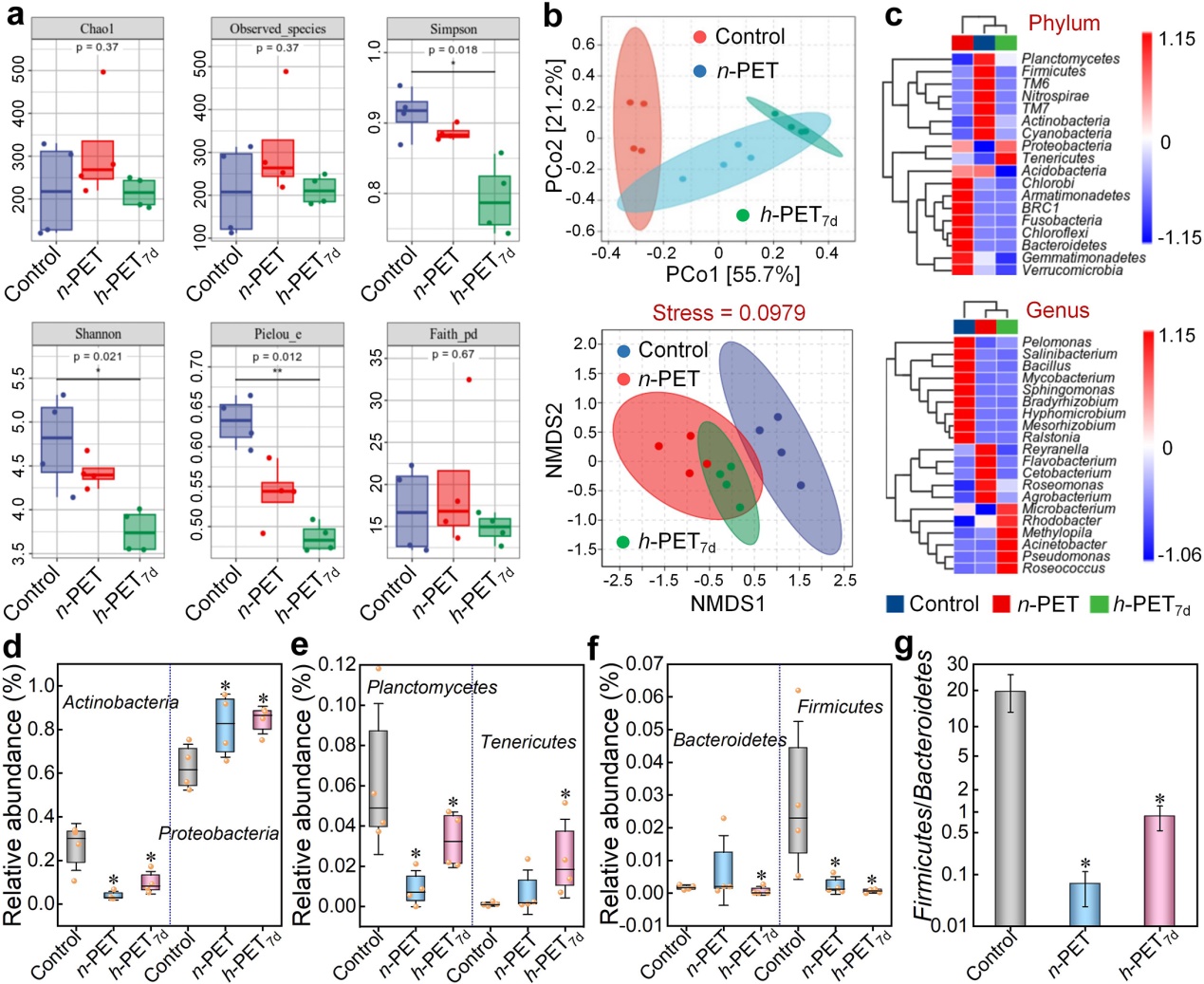
Fig.3. Evolution of intestinal microbiota following n-PET and h-PET7d exposure.
16S rRNA测序结果表明,h PET7d暴露显著降低了斑马鱼肠道菌群的α多样性,引起群落结构明显改变,而n PET对肠菌群的扰动程度相对较弱。具体而言,h PET7d诱导变形菌门(Proteobacteria)与软壁菌门(Tenericutes)相对丰度升高,厚壁菌门(Firmicutes)、放线菌门(Actinobacteria)、浮霉菌门(Planctomycetes)及拟杆菌门(Bacteroidetes)相对丰度明显降低,厚壁菌门/拟杆菌门比值显著下降,斑马鱼肠道菌群表现出致病菌过度繁殖与有益菌大量耗竭的失调特征。菌群功能预测进一步表明,h PET7d暴露导致短链脂肪酸合成及能量代谢相关通路下调,促进脂多糖(LPS)产生与细菌入侵上皮细胞能力相关通路上调。h-PET7d暴露引发的斑马鱼肠道菌群紊乱(LPS产生菌过度繁殖),为后续LPS入血诱发全身性炎症及肠 肝轴紊乱提供了菌群层面的直接证据。
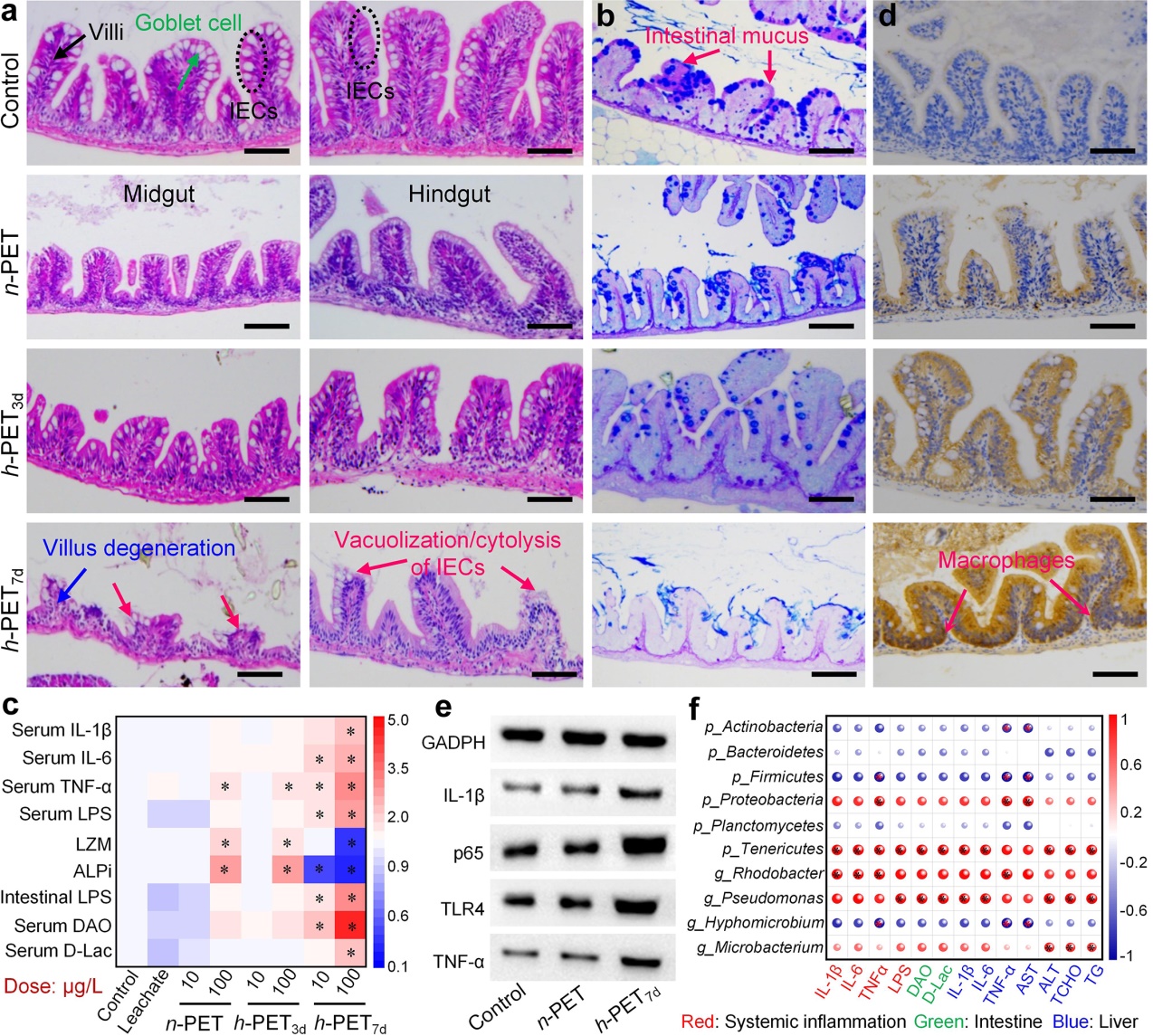
Fig.4. Intestinal damage and systemic inflammation in zebrafish exposed to MPs.
组织病理与生化分析表明,h PET7d暴露导致斑马鱼肠道绒毛萎缩、上皮细胞空泡化、杯状细胞减少及黏液层变薄,提示肠道组织结构损伤与屏障功能受损。血清中D 乳酸及二胺氧化酶水平升高,进一步证实h PET7d暴露增强了肠道通透性。转录组学、qPCR、免疫印迹及ELISA分析发现,h PET7d暴露导致斑马鱼肠道组织TLR4、TNF α、IL 1β及NF κB基因的转录水平及蛋白表达均显著上调,肠道和血清中LPS、TNF α、IL 1β和IL 6含量大幅升高,表明h PET7d通过激活LPS/TLR4/NF κB通路诱导肠道炎症并引发了全身性炎症反应。相关性分析发现,肠道菌群失调、屏障功能损伤与全身炎症及肝脏脂肪沉积之间存在强关联,结合肝脏极少的PET富集及其与脂肪沉积的无相关性实验结果,本研究证实h PET7d扰乱肠道菌群稳态所引发的全身性炎症,是驱动下游肝脏炎症与脂肪变性发生的上游分子信号。
转录组学揭示h-PET通过引发胰岛素抵抗与脂肪从头合成诱导肝脂肪变性
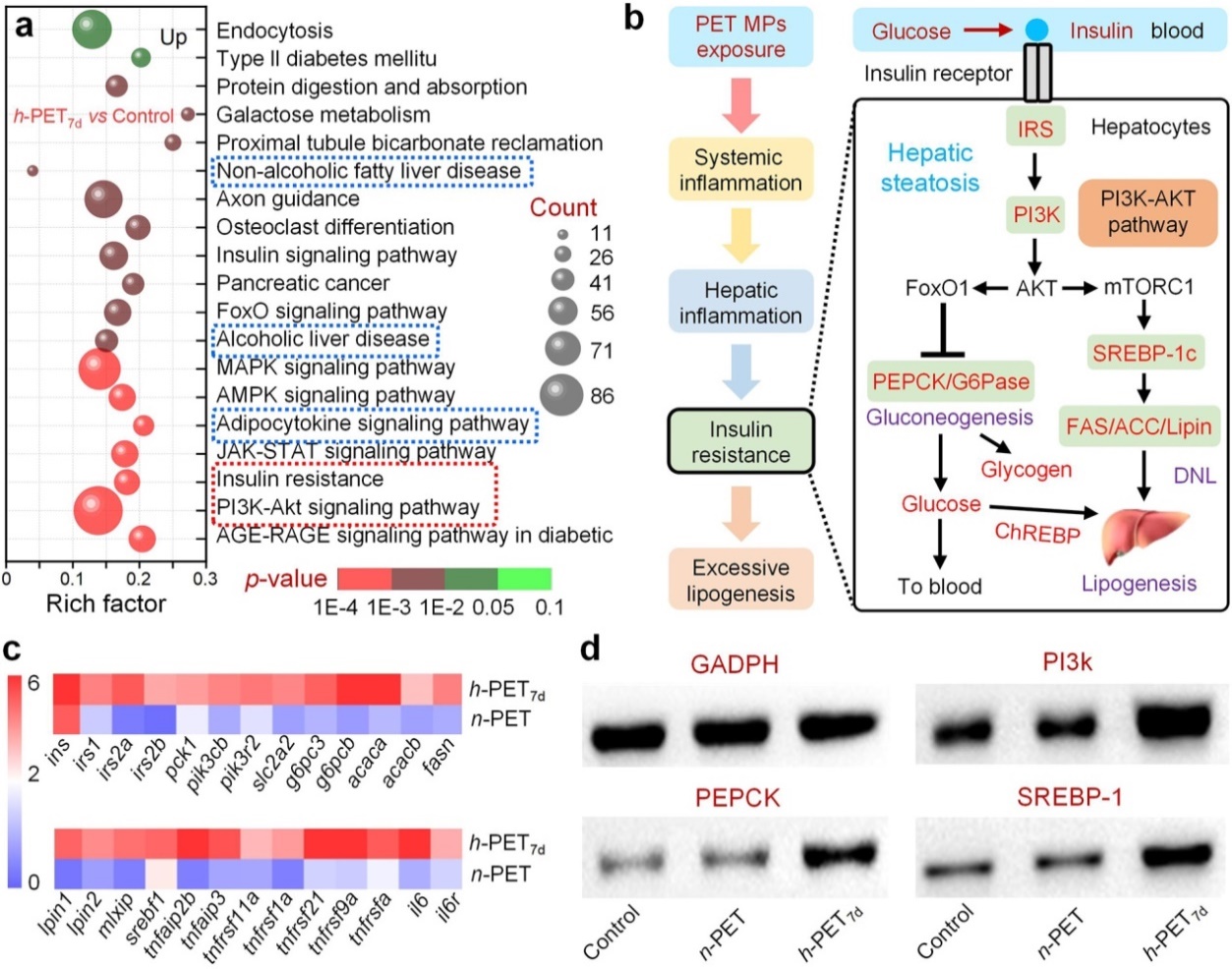
Fig. 5. Transcriptomic responses of zebrafish liver to n-PET and h-PET7d exposure.
转录组学分析显示,n-PET与h-PET7d对斑马鱼肝脏基因组表达的影响存在显著差异。n-PET主要下调与营养代谢及PPAR信号通路相关的基因,且未激活任何上调通路;而h-PET7d暴露导致2408个基因上调和1462个基因下调,并显著上调葡萄糖代谢、PI3K-Akt信号通路、胰岛素抵抗(insulin resistance, IR)以及脂肪肝病(包括酒精性肝病和非酒精性脂肪性肝病)相关通路。胰岛素在肝脏中的生理功能是抑制糖异生并促进脂质从头合成(de novo lipogenesis, DNL)。慢性炎症是IR发生发展的关键驱动力, IR状态下糖异生不再受到抑制而脂肪合成持续进行,导致甘油三酯和胆固醇过度蓄积最终形成脂肪肝。qPCR和免疫印迹验证进一步表明,h-PET7d通过激活肝脏IRS/PI3K/Akt轴,削弱FoxO1对糖异生的抑制作用;同时,通过上调转录因子ChREBP和SREBP-1c,促进乙酰辅酶A羧化酶(ACC)和脂肪酸合酶(FAS)的表达,从而驱动脂质从头合成。腹腔注射TLR4拮抗剂TAK-242以消除h-PET7d诱导的全身性炎症及肝脏炎症后,肝脏中acaca、fasn、srebf1基因的过表达以及脂质沉积均被逆转。综上所述,h-PET7d暴露通过以下级联通路诱导肝脏DNL和脂肪变性:“肠道菌群失调(LPS生成增多)→ 肠道LPS/TLR4/NF-κB炎症信号激活 → 肠道屏障损伤 → LPS及炎症因子入血 → 全身性炎症 → 胰岛素抵抗(IR)”。上述结果完整阐明了“肠-肝轴”紊乱在PET肝脏毒性中的核心机制。
膳食补充益生菌与丁酸钠通过改善肠道稳态缓解h-PET触发的全身炎症及肝脂肪变性
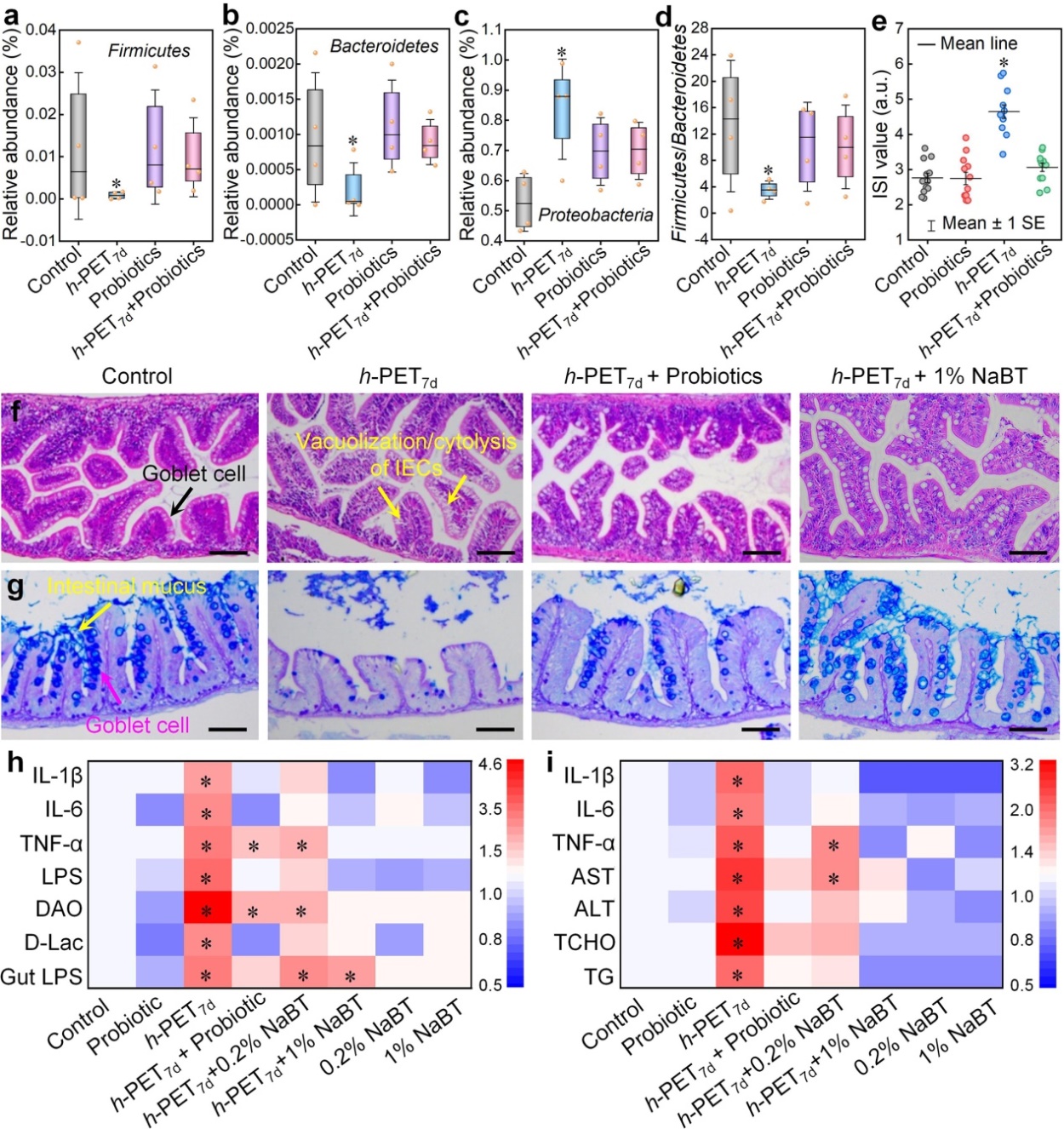
Fig.6. Intervention effects of probiotic LGG and NaBT on intestinal dysbiosis and hepatic damage of zebrafish induced by h-PET7d exposure.
膳食补充鼠李糖乳杆菌GG(LGG)显著逆转了h-PET7d诱导的肠道菌群失调,使厚壁菌门与拟杆菌门的比值恢复正常,缓解肠道绒毛萎缩及黏液层损伤,同时使血清中LPS及炎症因子水平回落至对照水平,最终消除肝脏脂质蓄积。补充丁酸钠(NaBT)虽未能改善h-PET7d暴露所致的肠道LPS含量升高,但通过上调紧密连接蛋白(cldng, cldnd, ZO-1和occludin)的表达增强了肠道屏障功能,从而有效阻断LPS入血所引发的全身性炎症及肝脏脂肪变性。上述结果再次证实了肠-肝轴紊乱在h-PET肝脏毒性中的核心地位,首次提出了靶向肠道微生态及屏障功能的可行干预策略,为微塑料相关代谢性疾病的防控提供了新思路。
结论与意义
这项工作首次阐明了瓶装水在不当热储存条件下释放的老化PET微塑料诱发肝脏脂肪变性风险的完整“肠-肝轴”毒性机制。研究不仅揭示了微塑料物理老化特征(粗糙度与粘附性增加)是驱动其肠道滞留与毒性增强的关键因素,还为应对微塑料污染引发的代谢性疾病提供了益生菌及丁酸盐干预的潜在解决方案,该成果为评估通过瓶装水摄入MPs的健康风险提供了重要科学依据。
论文链接
X. Zhang, R. Wang, M. Tang, C. Jin, G. Zhang, W. Zou, Suboptimal Thermal Storage Facilitates Aging of Bottle-Sourced Polyethylene Terephthalate Microplastics Fueling Hepatic Steatosis through Gut-Liver Axis Disruption, Environmental Science & Technology, 2026, 60, 9103-9116. https://doi.org/10.1021/acs.est.5c18229
备注: Permissions for reuse of all figures have been obtained from the original publisher. Copyright 2026, American Chemical Society.


